COMPOSICIÓN AGUA MAR DISOCIACIÓN
El 29 de Septiembre de 2021, la lava del volcán Cumbre Vieja de La Palma, llegó al mar…
COMPOSICIÓN DEL AGUA DEL MAR. DISOCIACIÓN EN QUÍMICA:

SE PRETENDE CON ESTA DINÁMICA EL DESARROLLO DE LAS COMPETENCIAS:
- COMPETENCIA MATEMÁTICA Y EN CIENCIA, TECNOLOGÍA E INGENIERÍA (STEM), concretamente los DESCRIPTORES OPERATIVOS STEM1 , STEM2 , STEM4
- COMPETENCIA EN CONCIENCIA Y EXPRESIÓN CULTURALES (CCEC), concretamente el DESCRIPTOR OPERATIVO CCEC2 y EL DESCRIPTOR OPERATIVO CCEC4.2
- COMPETENCIA EN COMUNICACIÓN LINGÜÍSTICA (CLL), concretamente los DESCRIPTORES OPERATIVOS CCL2 , CCL3.
- COMPETENCIA DIGITAL (CD), concretamente el DESCRIPTOR OPERATIVO CD1 y CD3
- COMPETENCIA EMPRENDEDORA (CE), concretamente el DESCRIPTOR OPERATIVO CE1
- COMPETENCIA PERSONAL, SOCIAL Y DE APRENDER A APRENDER (CPSAA), concretamente el DESCRIPTOR OPERATIVO CPSAA1.1 , CPSAA4 , CPSAA5
- COMPETENCIA PLURILINGÜE, concretamente los DESCRIPTORES OPERATIVOS CP1 , CP2
AGUA DE MAR:
El agua de mar es una disolución, de numerosos compuestos en agua, los cuales se encuentran en su mayoría en forma de iones, como consecuencia de la disociación de los productos químicos, naturales o no, que se aportan desde ríos, escorrentías, barrancos y de las numerosas fuentes consecuencia de la actividad humana e industrial.
Aunque con diferencias locales, el agua de mar es una disolución al 3,5% : en cada litro de agua (1000 gramos) hay 35 gramos de sales disueltas.
El ión cloruro (Cl–) es el que aparece en mayor proporción, en torno a un 55% del porcentaje de sus componentes disueltos, seguido del ión sodio (Na+), en torno a un 31 %. Ambos como consecuencia de la sal común (NaCl) disuelta en el agua de mar.
También presenta iones sulfato (SO42-), en torno a un 8% del total de solutos, como consecuencia de la disociación en el agua del los sulfatos sódicos y cálcicos que a él se aportan desde las rocas de los continentes.
En menor proporción tenemos disueltos iones magnesio (Mg++), Calcio (Ca++), iones bicarbonato (HCO3–), así como bromuros (Br–), Potasio (K+), flúor (F–) y otros compuestos, disociados o no, como el N2 y el CO2, que se encuentran en forma de gases en disolución. Contiene numerosos metales, algunos muy perjudiciales, productos de la actividad industrial, como mercurio, níquel, cobre, plomo, cromo…. Estos últimos pudiendo llegar a presentar concentraciones alarmantes en los últimos tiempos.
CUANDO LA LAVA LLEGA AL MAR:
Cuando la lava llega al mar, como consecuencia del efecto combinado de los propios gases contenidos en el interior de la lava, los elementos disueltos en el agua de mar y el choque entre la masa de lava a alta temperatura y el mar, se pueden producir compuestos que se emitan a la atmósfera perjudiciales para la salud, algunos de ellos, los característicos en la denominada “lluvia ácida”: HCl, H2SO4, óxidos de azufre y de nitrógeno.
El hecho de que la lava lleve gases en su interior, no nos debe sorprender, ya que en el interior de la Tierra hay gases. Se sabe que en las minas de Carbón existe un gas muy peligroso, el grisú, cuyo componente principal es el metano (CH4), que puede producir explosiones. Como curiosidad, antes de la existencia de dispositivos sofisticados que detectan el gas, los mineros llevaban una jaula con un pájaro, un canario (que es muy sensible a la presencia de los gases), que si se observaba un comportamiento inquieto, indicaba la posible presencia de gases nocivos.
En el interior de la lava también existe ácido sulfídrico (SH2) que tiene un característico olor a huevos podridos, que los vecinos de La Palma, han podido detectar, como se ha indicado incluso en las noticias.
En la lava también existe dióxido de azufre u óxido de azufre (IV), que se podría oxidar a trióxido de azufre, pudiendo éste último en presencia de agua producir ácido sulfúrico, según la siguiente cadena de reacciones:
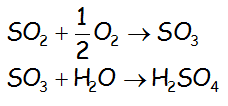
Es más que evidente la contribución del ácido sulfúrico a la lluvia ácida.
Nos conviene en todos estos procesos que juegan un papel importante en el medio natural, hablar un poco de la disociación de los compuestos químicos, por lo que veremos a continuación:
DISOCIACIÓN DE COMPUESTOS QUÍMICOS:
La disociación es un proceso en el cual determinados compuestos se separan en iones. Tal cuestión es de mucho interés, ya que en la mayor parte de los casos, las reacciones se producen en disolución, estando los intervinientes en la misma, en estado iónico.
Existen compuestos que en general NO SE DISOCIAN:
Los elementos en su estado fundamental, como el H2, O2, N2, Cl2…
Las combinaciones con el oxígeno como los óxidos, anhídridos y peróxidos: FeO, Cl2O3, H2O2, …
Los compuestos que SI SE DISOCIAN, tienen las siguientes tendencias a la hora de disociarse:
Los hidruros (metálicos y no metálicos):
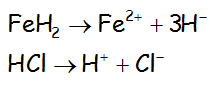
Notar como el hidrógeno en el caso de los hidruros metálicos resulta un anión y en los no metálicos da lugar a un catión.
Las sales binarias:
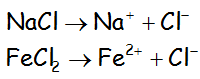
Los oxoácidos:
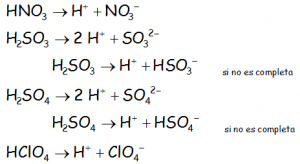
Las sales oxoácidas, tanto neutras como ácidas:
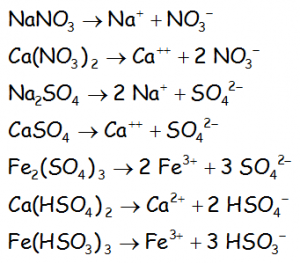
Los hidróxidos:
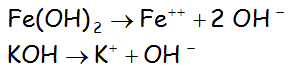
Para poder nombrar e incluso comprender mejor el proceso de disociación, así como las cargas de los iones que intervienen, puede resultar de interés, consultar el siguiente enlace, del cuadernillo de formulación inorgánica:
CUADERNILLO DE FORMULACIÓN INORGÁNICA
EJERCICIO FQ1BE2161;
Las siguientes reacciones químicas no se encuentran ajustadas. Para cada una de ellas, intentar un ajuste por tanteo y escribir la reacción en forma iónica, esto es, disociando los compuestos presentes susceptibles de ello en los correspondientes iones, que son al fin y al cabo los que participan en la reacción:
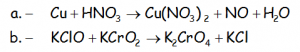
PODRÍA INTERESAR VER EL SIGUIENTE ENLACE DE ESTA MISMA WEB: LA MAGIA DEL VOLCÁN