TERMOQUÍMICA HESS QUÍMICA BACHILLERATO
TERMOQUÍMICA, PARA QUÍMICA DE BACHILLERATO. RECURSOS AUDIOVISUALES:

ASPECTOS FORMALES PARA DOCENTES AL FINAL DEL ARTÍCULO, PARA NO INTERFERIR CON LO QUE ES DE INTERÉS PARA LOS ALUMNOS.
PUEDE INTERESAR LA CONSULTA DE LOS SIGUIENTES ARTÍCULOS:
ESTÁ EN CONSONANCIA CON LAS ESTRATEGIAS DETERMINADAS POR LAS PROPUESTAS DE PROGRAMACIONES DIDÁCTICAS:
EJERCICIO F1BE2076:
Teniendo en cuenta la siguiente reacción, de formación del agua, en la que se incluye la entalpía correspondiente:
H2 + 1/2 O2 → H2O ; ΔH = – 300 kJ
a.- Hallar la energía que se desprende cuando se forman 2 moles de agua.
b.- Hallar la energía que se desprende cuando se forman 4 gramos de agua.
c.- Hallar la masa de agua que se tiene que formar para que se desprendan 1500 kJ.
DATOS DE MASAS ATÓMICAS EN U.M.A.: Ma(H)=1; Ma(O)=16
VÍDEO QUE RESUELVE EL EJERCICIO: https://youtu.be/6t_UP4bLDF0
EJERCICIO F1BE2077:
Teniendo en cuenta la siguiente reacción, de formación del agua, en la que se incluye la entalpía correspondiente:
H2 + 1/2 O2 → H2O ; ΔH = – 300 kJ
Hallar la energía que se desprende cuando se intenta formar agua con 5 g de hidrógeno y 5 gramos de oxígeno.
DATOS DE MASAS ATÓMICAS EN U.M.A.: Ma(H)=1; Ma(S)=32 ; Ma(O)=16
SOLUCIÓN: Se desprenden 93,75 kJ
EJERCICIO FQ1BE2090:
Sabiendo que la entalpía de combustión del etanol es -764 kJ/mol.
a.- Escribir y ajustar la reacción de combustión del etanol, añadiendo la entalpía correspondiente, lo que la convierte en una ecuación termoquímica.
b.- Con lo que se ha aportado, indicar si la reacción de combustión del etanol es exotérmica o endotérmica.
c.- Con lo que se ha aportado, indicar si en la combustión del etanol, se absorbe o se desprende energía.
d.- Hallar la energía que se desprende o se absorbe cuando se realiza la combustión de 25 gramos de etanol.
DATOS DE MASAS ATÓMICAS EN U.M.A.: C=12; H=1; O=16.
DIAGRAMAS DE ENTALPÍA. COMPARATIVA DE LOS DIAGRAMAS ENTÁLPICOS DE REACCIONES EXOTÉRMICAS Y ENDOTÉRMICAS.
Notar en las gráficas que se muestran, el hecho de que el valor de la variación de entalpía de la reacción en sentido inverso, cambia el signo. Si una reacción es endotérmica en un sentido, sería exotérmica en sentido inverso. Se muestran las reacciones que participan en el motor y en la pila de hidrógeno.
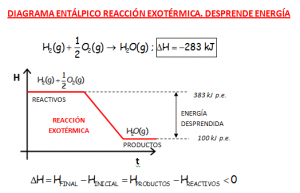
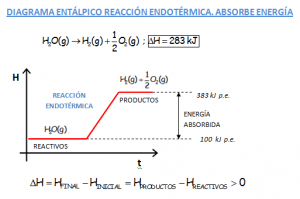
Ir al vídeo que explica lo indicado en las gráficas que se muestran: https://youtu.be/lmpYkg13Yi4
ENTALPÍA DE REACCIÓN A TRAVÉS DE LA LEY DE HESS:
LEY DE HESS:
«Si una reacción puede producirse en varias etapas, su variación de entalpía es igual a la suma de las entalpías de reacción de estas reacciones intermedias».
O lo que es lo mismo: si una reacción R, puede considerarse como suma de otras reacciones: A, B, C, D, … , se cumplirá que:
ΔHR = ΔHA + ΔHB + ΔHC + ΔHD + …
«El cambio de energía calórica que acompaña a una reacción química a Volumen y presión constante, es independiente del número y naturaleza de los estados intermedios».
A un nivel operativo, podemos atrevernos a decir que: «cuando una reacción es combinación de otras reacciones, su entalpía es la combinación de las entalpías de las otras reacciones». Lo mejor será verlo en un ejemplo.
EJERCICIO F1BE2079:
Hallar la entalpía de la siguiente reacción:
C(s) + O2 (g) → CO2 (g)
Conociendo las entalpías de las reacciones:
CO(g) + 1/2 O2(g) → CO2(g) ; ΔH = – 283,0 kJ
C(s) + 1/2 O2(g) → CO(g) ; ΔH = – 110,5 kJ
IR AL VÍDEO QUE RESUELVE EL EJERCICIO UTILIZANDO LA LEY DE HESS: https://youtu.be/8iSQMMITJto
EJERCICIO FQ1BE1205:
El metanol se obtiene industrialmente a partir de monóxido de carbono e hidrógeno según la reacción:
CO(g) + 2 H2(g) → CH3OH(g)
Calcular el cambio de entalpía para la reacción de síntesis industrial de metanol, teniendo en cuenta las siguientes ecuaciones termoquímicas:
CO(g) + 1/2 O2(g) → CO2(g) ; ΔHo = – 283,0 kJ
CH3OH(g) + 3/2 O2(g) → CO2(g) + 2 H2O(g) ; ΔHo = – 764,4 kJ
H2(g) + 1/2 O2(g) → H2O(g) ; ΔHo = – 285,8 kJ
IR AL VÍDEO QUE RESUELVE EL EJERCICIO CON LA LEY DE HESS: https://youtu.be/Q0EgfPM8Zfg
ENTALPÍA DE REACCIÓN A TRAVÉS DE LAS ENTALPÍAS DE FORMACIÓN:
La entalpía normal de formación de un compuesto en condiciones estándar, también denominada calor de formación, se representará por ΔHºf, y se define como: el cambio de entalpía (variación de calor), ΔH, que tiene lugar cuando se forma un mol de compuesto a partir de los elementos que lo constituyen en sus estados de agregación más estables en condiciones estándar (1 atm de presión y 25º C de temperatura).
Con estos datos de entalpías normales de formación, podemos calcular la entalpía normal (en condiciones estándar) de una reacción, utilizando:
ΔH0reacción=Σnp·ΔHºf p – Σnr·ΔHºf r
Donde np y nr hacen referencia a los coeficientes estequiométricos de los productos y de los reactivos; ΔHºf p y ΔHºf r son las entalpías normales de formación de los productos y reactivos respectivamente.
«A la entalpía estándar de formación de los elementos en su estado estándar se les asigna la entalpía cero», ya que su formación no supone ningún proceso químico.
Algunos elementos en estado estándar, por lo tanto con entalpía de formación estándar con valor cero: O2 (g); C (grafito); H2 (g); Br2 (l); Fe (s); S (s); P (blanco); Hg (l); Al (s); Ca (s);
EJERCICIO FQ1BE427:
La entalpía estándar de formación de la glucosa (C6H12O6) es -1268 kJ/mol. La entalpía estándar de formación del agua líquida es -187,78 kJ/mol y la del anhídrido carbónico es -393,51 kJ/mol.
a.- Hallar la entalpía de combustión estándar de la glucosa.
b.- Indicar si la reacción de combustión es exotérmica o endotérmica.
c.- Hallar el calor asociado a la combustión de 8 gramos de glucosa.
SOLUCIÓN: -2219,74 kJ
EJERCICIO FQ1BE3113:
La entalpía estándar de formación de la glucosa es –1 268 kJ/mol. La entalpía estándar de formación del agua líquida es –187,78 kJ/mol, y del CO2, –393,51 kJ/mol.
a) Calcula la entalpía de formación de glucosa en la fotosíntesis,
6 CO2(g) + 6 H2O(l) → C6H12O6(s) + 6 O2(g),
b) ¿La reacción es exotérmica o endotérmica?
SOLUCIÓN: 2219,74 kJ
EJERCICIO FQ1BE3114:
Calcula la entalpía de formación estándar del óxido de nitrógeno (V) a partir de las siguientes ecuaciones termoquímicas:
4 NO2 (g) + O2 (g) → 2 N2O5 (g) , ΔHº = – 110,2 kJ
1/2 N2 (g) + 1/2 O2 (g) → NO (g) , ΔHº = 90,25 kJ
2 NO (g) + O2 (g) → 2 NO2 (g) , ΔHº = – 114,1 kJ
SOLUCIÓN: 11,3 kJ
EJERCICIO FQ1BE3115:
Calcula la entalpía de la siguiente reacción, de reducción del hierro (II):
FeO (s) + CO (g) → Fe (s) + CO2 (g),
a partir de las siguientes ecuaciones termoquímicas:
Fe2O3 (s) + 3 CO (g) → 2 Fe (s) + 3 CO2 (g) , ΔHº = – 24,7 kJ
Fe3O4 (s) + CO (g) → 3 FeO (s) + CO2 (g) , ΔHº = 35,9 kJ
3 Fe2O3 (s) + CO (g) → 2 Fe3O4 (s) + CO2 (g) , ΔHº = – 47,2 kJ
SOLUCIÓN: -16,45 kJ
EJERCICIO FQ1BE3116:
A.- Calcula la entalpía de formación del acetileno (etino):
2 C (s) + H2 (g) → C2H2 (g)
a partir de las siguientes ecuaciones termoquímicas:
a) 2 C2H2 (g) + 5 O2 (g) → 4 CO2 (g) + 2 H2O (l) , ΔH°= –2600 kJ
b) C (s) + O2 (g) → CO2 (g) , ΔH° = –394 kJ
c) 2 H2 (g) + O2 (g) → 2 H2O (g) , ΔH° = –483,6 kJ
d) H2O (l) → H2O (g) , ΔH° = +44 kJ
B.- Para la reacción de combustión del acetileno, que tienes que identificar entre las que se muestran, indicar si es exotérmica o endotérmica, si se desprende o se absorbe calor y obtener el calor que se intercambia cuando se obtienen dos moles de anhídrido carbónico.
IR AL ARTÍCULO CON LA RESOLUCIÓN DEL EJERCICIO: EXAMEN RESUELTO DE REACCIONES QUÍMICAS Y TERMOQUÍMICA, PARA FÍSICA Y QUÍMICA DE 1º DE BACHILLERATO. PRUEBA 2 DEL TERCER TRIMESTRE DEL CURSO 2025-26. PRUEBA COMPETENCIAL
EJERCICIO FQ1BE3117:
a.- Calcula la entalpía de reacción estándar para la reacción de hidrogenación del etino a eteno:
C2H2 (g) + H2 (g) → C2H4 (g)
a partir de los siguientes datos termoquímic0s:
2 C2H4 (g) + 6 O2 (g) → 4 CO2 (g) + 4 H2O (l) , ΔH°= –2822 kJ
2 H2 (g) + O2 (g) → 2 H2O (l) , ΔH°= –572 kJ
2 C2H2 (g) + 5 O2 (g) → 4 CO2 (g) + 2 H2O (l) , ΔH°= –2600 kJ
b.- Para la reacción de combustión del etino , hallar la energía que se intercambia (indicando si se desprende o se absorbe), cuando se queman 50 g de etino.
DATOS: Ma(C)=12 u; Ma(O)=16 u; Ma(H)=1 u
EJERCICIO FQ1BE3118:
Calcular la entalpía estándar de la siguiente reacción:
C2H2 (g) + 2 H2 (g) → C2H6 (g)
a partir de las siguientes ecuaciones termoquímicas:
H2 (g) + 1/2 O2 (g) → H2O (l) , ΔH°= –286 kJ
2 C2H2 (g) + 5 O2 (g) → 4 CO2 (g) + 2 H2O (l) , ΔH°= –2600 kJ
2 C2H6 (g) + 7 O2 (g) → 4 CO2 (g) + 6 H2O (l) , ΔH°= –3120 kJ
SOLUCIÓN: – 312 kJ
EJERCICIO FQ1BE3119:
En la obtención de ácido sulfúrico, las industrias utilizan la combustión del azufre y la oxidación del dióxido de azufre. a partir de los datos siguientes,
S (s) + O2 (g) → SO2 (g) , ΔH°= –297 kJ
2 S (s) + 3 O2 (g) → 2 SO3 (g) , ΔH°= –791 kJ
Calcúlese la entalpía de reacción de la oxidación de SO2 a SO3,
2 SO2 (g) + O2 (g) → 2 SO3 (g)
SOLUCIÓN: – 197 kJ
EJERCICIO FQ1BE3120:
Obtener la variación de entalpía estándar de la reacción de formación del cloruro de aluminio anhidro,
2 Al (s) + 3 Cl2 (g) → 2 AlCl3 (s) ,
teniendo en cuenta las siguientes reacciones, en las que se añaden datos termoquímicos:
H2 (g) + Cl2 (g) → 2 HCl (g) , ΔH°= –185 kJ
2 Al (s) + 6 HCl (aq) → 2 AlCl3 (aq) + 3 H2 (g) , ΔH°= –1049 kJ
HCl (g) → HCl (aq) , ΔH°= –78,4 kJ
AlCl3 (s) → AlCl3 (aq) , ΔH°= –323 kJ
SOLUCIÓN: -1428,4 kJ
EJERCICIO FQ1BE3121:
Obtener la variación de entalpía estándar de la reacción de formación del ácido clorhídrico gaseoso a partir de hidrógeno y cloro gaseosos, considerando los siguientes datos aportados por ecuaciones termoquímicas:
NH3 (g) + HCl (g) → NH4Cl (s) , ΔH°= –176 kJ
N2 (g) + 4 H2 (g) + Cl2 (g) → 2 NH4Cl (s) , ΔH°= –629 kJ
N2 (g) + 3 H2 (g) → 2 NH3 (g) , ΔH°= –92 kJ
SOLUCIÓN: -185 kJ
EJERCICIO FQ1BE3122:
Calcular la variación de entalpía estándar de la reacción:
2 CH4(g) + 3 O2(g) → 2 CO (g) + 4 H2O (l), teniendo en cuenta los siguientes datos:
CH4(g) + 2 O2(g) → CO2 (g) + 2 H2O (l) , ΔH°= –890 kJ
2 CO (g) + O2(g) → 2 CO2 (g) , ΔH°= –566 kJ
SOLUCIÓN: -1214 kJ
EJERCICIO FQ1BE3123:
Calcular la variación de entalpía estándar para la reducción de hidrazina a amoníaco, según la siguiente reacción:
N2H4 (l) + H2 (g) → 2 NH3 (g),
a partir de las siguientes reacciones termoquímicas:
N2 (g) + 2 H2 (g) → N2H4 (l), ΔH°= 50,6 kJ
N2 (g) + 3 H2 (g) → 2 NH3 (g), ΔH°= -92,2 kJ
SOLUCIÓN: -142,8 kJ
EJERCICIO Q2BE1574:
Calcular el calor de formación del ácido metanoico líquido, a partir de los siguientes calores de reacción. Indicar el resultado en Julios y calorías, añadiendo si la reacción en endotérmica o exotérmica y si absorbe o desprende calor:
C (s) + ½ O2 (g) → CO (g) ; ΔH = –110,4 kJ
H2 (g) + ½ O2 (g) → H2O (l) ; ΔH = –285,5 kJ
CO (g) + ½ O2 (g) → CO2 (g) ; ΔH = –283,0 kJ
HCOOH(l) + ½ O2 (g) → H2O (l) + CO2 (g) ; ΔH = –259,6 kJ
DATO: 1 J = 0,24 cal
IR A LA RESOLUCIÓN DEL EJERCICIO: EJERCICIO RESUELTO DE TERMOQUÍMICA. APLICACIÓN DE LA LEY DE HESS PARA OBTENER EL CALOR DE FORMACIÓN DEL ÁCIDO METANOICO. QUÍMICA DE BACHILLERATO
EJERCICIO Q2BE1843:
Si cuando se forma 1,0 gramo de metanol se desprenden 7,46 kJ, calcular:
a.- ¿Cuál será el valor de su entalpía de formación?
b.- ¿Cuál será la entalpía estándar de combustión del metanol, sabiendo que el agua que se forma es líquida?
DATOS: Ma(C)=12 u; Ma(O)=16 u; Ma(H)=1 u; Entalpías estándar de formación del CO2 (g) y del H2O (l) respectivamente: -393,8 kJ/mol y -285,8 kJ/mol
SOLUCIÓN: -238,72 kJ/mol; -726,68
EJERCICIO Q2BE1198:
Calcular la entalpía de formación del óxido de cinc a partir de los siguientes datos:
H2SO4 (aq) + ZnO (s) → ZnSO4 (aq) + H2O (l) ; ΔH = – 210 kJ
H2SO4 (aq) + Zn (s) → ZnSO4 (aq) + H2 (g) ; ΔH = – 335 kJ
2 H2 (g) + O2 (g) → 2 H2O (l) ; ΔH = – 571 kJ
SOLUCIÓN: -410,5 kJ
EJERCICIO Q2BE1199:
Calcula la entalpía de formación del tricloruro de aluminio teniendo en cuenta estos datos:
2 Al (s) + 6 HCl (aq) → 2 AlCl3 (aq) + 3 H2 (g) ; ΔH = – 1062 kJ
H2 (g) + Cl2 (g) → 2 HCl (g) ; ΔH = – 184,6 kJ
HCl (g) → HCl (aq) ; ΔH = – 73 kJ
AlCl3 (s) → AlCl3 (aq) ; ΔH = – 326 kJ
IR A LA RESOLUCIÓN DEL EJERCICIO: EJERCICIO RESUELTO DE TERMOQUÍMICA. APLICACIÓN DE LA LEY DE HESS PARA OBTENER EL CALOR DE FORMACIÓN DEL TRICLORURO DE ALUMINIO. QUÍMICA DE BACHILLERATO
EJERCICIO Q2BE1201:
a.- Calcula la entalpía de formación del gas monóxido de nitrógeno, a partir de nitrógeno y oxígeno gaseosos, teniendo en cuenta estos datos:
N2 (g) + 3 H2 (g) → 2 NH3 (g) ; ΔH = – 92,2 kJ
2 H2 (g) + O2 (g) → 2 H2O (l) ; ΔH = – 571 kJ
2 NH3 (g) + 5/2 O2 (g) → 2 NO (g) + 3 H2O (l) ; ΔH = – 584,8 kJ
b.- través de la ecuación correspondiente, de entre las que se muestran, hallar el calor que se intercambia (indicando si se absorbe o se desprende) cuando pretendemos obtener 6,022 · 10 23 moléculas de amoniaco, a partir de nitrógeno y oxígeno gaseosos.
DATOS: N.A.=6,022 · 10 23 mol -1
IR A LA RESOLUCIÓN DEL EJERCICIO: EJERCICIO RESUELTO DE TERMOQUÍMICA. APLICACIÓN DE LA LEY DE HESS PARA OBTENER EL CALOR DE FORMACIÓN DEL MONÓXIDO DE NITRÓGENO. QUÍMICA DE BACHILLERATO
EJERCICIO Q2BE1200:
a.- Calcula la entalpía molar de formación del ácido nitroso disuelto, teniendo en cuenta que la entalpía de formación del agua líquida es -68,3 kcal/mol y los siguientes datos de entalpías de reacción que se aportan:
NH4NO2 (aq) → N2 (g) + 2 H2O (l) ; ΔH = – 76,5 kcal
NH3 (aq) + HNO2 (aq) → NH4NO2 (aq) ; ΔH = – 9 kcal
2 NH3 (aq) → N2 (g) + 3 H2 (g) ; ΔH = 40,6 kcal
SOLUCIÓN: ? -30,8 kcal/mol
b.- Con el resultado de la entalpía obtenido anteriormente responder a las siguientes preguntas:
b.1.- Hallar el calor que se desprende (o que se necesita) para obtener 1 kg de ácido nitroso disuelto.
b.2.- Hallar la energía (en Julios) que se obtiene (o que se necesita) cuando pretendemos obtener ácido nitroso disuelto partiendo de 5 gramos de nitrógeno, 5 gramos de hidrógeno y 5 gramos de oxígeno.
ACLARACIONES PARA LA REALIZACIÓN DEL EJERCICIO:
La ENTALPÍA MOLAR DE FORMACIÓN de un compuesto químico es la entalpía asociada a la formación de un mol de ese compuesto, partiendo de los elementos que lo componen en su estado de agregación más estable. Esto supone en nuestro caso, que la reacción del formación del acido nitroso parte de oxígeno, nitrógeno e hidrógeno gases (diatómicos) y que el ajuste de la reacción no puede modificar que nos dé como resultado un mol de ácido nitroso.
El dato de la entalpía de formación del agua líquida corresponde a una reacción que sigue los mismos parámetros que comentamos en el párrafo anterior.
Tener en cuenta que 1 Julio = 0,24 calorías.
Para el apartado b.2 razonar de forma adecuada con los reactivos al respecto de REACTIVO LIMITANTE Y EN EXCESO (¡ TRES REACTIVOS !) ya que alguno o más podrían estar en exceso.
Parte de la solución a este apartado: Reaccionarán 0,15625 g de hidrógeno; 2,1875 g de nitrógeno y 5 gramos de oxígeno.
PODRÍA INTERESAR LA CONSULTA DE LOS SIGUIENTES RECURSOS DE QUÍMICA 2º BACHILLERATO:
EJERCICIOS DE TERMOQUÍMICA CON SOLUCIÓN
MATERIALES DE QUÍMICA DE 2º BACHILLERATO
ASPECTOS FORMALES PARA DOCENTES:
SE PRETENDE CON ESTA DINÁMICA EL DESARROLLO DE LAS COMPETENCIAS:
- COMPETENCIA MATEMÁTICA Y EN CIENCIA, TECNOLOGÍA E INGENIERÍA (STEM), concretamente los DESCRIPTORES OPERATIVOS STEM1 , STEM2 , STEM4
- COMPETENCIA EN CONCIENCIA Y EXPRESIÓN CULTURALES (CCEC), concretamente el DESCRIPTOR OPERATIVO CCEC2 y EL DESCRIPTOR OPERATIVO CCEC4.2
- COMPETENCIA EN COMUNICACIÓN LINGÜÍSTICA (CLL), concretamente los DESCRIPTORES OPERATIVOS CCL2 , CCL3.
- COMPETENCIA DIGITAL (CD), concretamente el DESCRIPTOR OPERATIVO CD1 y CD3
- COMPETENCIA EMPRENDEDORA (CE), concretamente el DESCRIPTOR OPERATIVO CE1
- COMPETENCIA PERSONAL, SOCIAL Y DE APRENDER A APRENDER (CPSAA), concretamente el DESCRIPTOR OPERATIVO CPSAA1.1 , CPSAA4 , CPSAA5
- COMPETENCIA PLURILINGÜE, concretamente los DESCRIPTORES OPERATIVOS CP1 , CP2