QUÍMICA ÁTOMO TABLA PERIÓDICA
FÍSICA QUÍMICA SECUNDARIA
QUÍMICA BÁSICA, ESTRUCTURA DEL ÁTOMO, TABLA PERIÓDICA, PARA FÍSICA Y QUÍMICA DE SECUNDARIA:

PUEDE INTERESAR LA CONSULTA DE LOS SIGUIENTES MATERIALES RELACIONADOS:
ESTE MATERIAL SIGUE LOS PROCESOS DETERMINADOS POR:
-
- FÍSICA Y QUÍMICA DE 2º DE LA ESO. DESARROLLO DE LA ASIGNATURA
- FÍSICA Y QUÍMICA DE 3º DE LA ESO. DESARROLLO DE LA ASIGNATURA
- FÍSICA Y QUÍMICA DE 4º DE LA E.S.O.: DESARROLLO DE LA ASIGNATURA
- FÍSICA Y QUÍMICA DE 1º DE BACHILLERATO: DESARROLLO DE LA ASIGNATURA
- QUÍMICA DE 2º BACHILLERATO: DESARROLLO DE LA ASIGNATURA
En esta entrada pretendemos dar las nociones básicas que nos acercan a la química: de la estructura del ÁTOMO, de su relación con la colocación en la TABLA PERIÓDICA, no sólo de masas crecientes, sino de las características de combinación de unos elementos con otros (la VALENCIA), así como material para nombrar adecuadamente los compuestos. Pretende ser una clase introductoria a QUÍMICA de Secundaria y aclaratoria para los primeros cursos de Bachillerato. A medida que seguimos avanzando en química en cursos posteriores, todo esto se amplía y se justifica.
SE PRETENDE CON ESTA DINÁMICA EL DESARROLLO DE LAS COMPETENCIAS:
- COMPETENCIA MATEMÁTICA Y EN CIENCIA, TECNOLOGÍA E INGENIERÍA (STEM), concretamente los DESCRIPTORES OPERATIVOS STEM1 , STEM2 , STEM4
- COMPETENCIA EN CONCIENCIA Y EXPRESIÓN CULTURALES (CCEC), concretamente el DESCRIPTOR OPERATIVO CCEC2 y EL DESCRIPTOR OPERATIVO CCEC4.2
- COMPETENCIA EN COMUNICACIÓN LINGÜÍSTICA (CLL), concretamente los DESCRIPTORES OPERATIVOS CCL2 , CCL3.
- COMPETENCIA DIGITAL (CD), concretamente el DESCRIPTOR OPERATIVO CD1 y CD3
- COMPETENCIA EMPRENDEDORA (CE), concretamente el DESCRIPTOR OPERATIVO CE1
- COMPETENCIA PERSONAL, SOCIAL Y DE APRENDER A APRENDER (CPSAA), concretamente el DESCRIPTOR OPERATIVO CPSAA1.1 , CPSAA4 , CPSAA5
- COMPETENCIA PLURILINGÜE, concretamente los DESCRIPTORES OPERATIVOS CP1 , CP2
SE CONTEMPLAN LOS ASPECTOS RELACIONADOS CON EL PERFIL DE SALIDA DEL ALUMNADO DE LOS INSTITUTOS DIOCESANOS DE CANARIAS
Independientemente de lo que se añade en la entrada, puede resultar interesante visualizar el video siguiente, en formato clase, de esto que estamos intentando trasladar:
VIDEO EN FORMATO CLASE ON-LINE DE ESTRUCTURA DE LA MATERIA, QUÍMICA BÁSICA: PROTONES, NEUTRONES, ELECTRONES, VALENCIA:
CLASE ON-LINE QUIMBAS01: https://youtu.be/BnufWqffTxc
Por qué se intercambian las valencias de los elementos en los compuestos químicos: https://youtu.be/ZC8ElD7ATcE
Dalton a comienzos del siglo XIX, decía que la materia estaba formada por partículas indivisibles, que llamó átomos. Sabemos que el átomo está formado por partículas que se encuentran en su interior, en el núcleo, que son los PROTONES y NEUTRONES. En el exterior del átomo, en la corteza, se encuentran los ELECTRONES. Por lo tanto, sí que es divisible el átomo, pero no por ello Dalton estaba desencaminado.
Las masas de estas partículas son similares para el protón y el neutrón que son en torno a 2000 veces mayor que los electrones.
Los protones tienen la misma carga que los electrones, sólo que los protones son positivos y los electrones negativos. Es por ello por lo que si un átomo tiene el mismo número de protones que de electrones, entonces es neutro.
Si tocamos el núcleo, la hemos fastidiado, bomba atómica, energía nuclear. Estas partículas del núcleo, los protones y los neutrones están fuertemente unidas. Cuando rompemos el núcleo y se forman núcleos más pequeños, proceso de fisión nuclear, se libera mucha energía, que es la que aprovechan las centrales nucleares para producir energía eléctrica. En las estrellas ocurre fusión nuclear (se forman núcleos más grandes fusionando núcleos de átomos más pequeños), también libera mucha energía. La química está determinada básicamente por causa de los electrones que se puede decir que van y vienen de unos elementos a otros, o se comparten.
Lo que aparece en la tabla periódica son elementos, cuando éstos se unen forman compuestos. Un elemento es distinto de otro por causa de los protones que tiene. El Litio es litio porque tiene 3 protones en el núcleo, si tuviera cuatro sería entonces Berilio, no Litio. Sin embargo, dentro de unos valores razonables hay litio con 3 neutrones, con cuatro… y el Litio puede perder alguno de los tres electrones que normalmente tiene si está en estado neutro.
El NÚMERO ATÓMICO «Z» es el número de protones que tiene el núcleo, que coincide con el número de electrones si el átomo es neutro.
Los átomos que tienen el mismo número atómico, corresponden al mismo elemento químico.
El NÚMERO MÁSICO «A» es la suma de protones y de neutrones, la suma de las partículas del núcleo, que casi que coincide con la masa atómica del átomo, ya que la masa de los electrones es despreciable frente a las dos partículas gordas que tiene el núcleo.
ISÓTOPO
Se denomina isótopo a los átomos que tienen el mismo número atómico, pero tienen diferente el número másico. Son el mismo elemento químico, sólo que con un número de neutrones diferente.
Dependiendo de los orbitales atómicos (pisos o niveles donde se sitúan los electrones), los distintos elementos tienen tendencias marcadas para perder o ganar un número determinado de ellos, que determinan la valencia, así como el ión al que dan lugar, positivo o negativo. Los electrones, cuanto más alejados están del núcleo tienen menor energía, por lo tanto es más fácil perderlos (están menos ligados al núcleo).
Los elementos no pierden protones, ni los ganan. Pierden o ganan electrones. Si un elemento neutro gana un electrón se convierte en un IÓN NEGATIVO (anión); si pierde un electrón, se convierte en un IÓN POSITIVO (catión), lógico teniendo en cuenta el exceso de cargas que tiene.
Si conocemos el número atómico, podemos por lo tanto saber el número de electrones que tiene el átomo, si nos indican si el átomo es neutro o un ión positivo o negativo.
Estas tendencias quedan reflejadas en la tabla periódica y determinan el comportamiento químico de los elementos a la hora de combinarse unos con otros para formar compuestos.
La VALENCIA tiene mucho que ver con los electrones que el átomo «desea» ganar o perder… y determina en una medida importante, con quién desea un elemento unirse con otro, para formar un compuesto estable en las condiciones en las que existe.
O lo que es lo mismo, la VALENCIA tiene mucho que ver con los electrones que le faltan (o que le sobran) a un elemento para parecerse al gas noble más cercano.
Sería fantástico que el alumno que comienza con química memorizara los elementos de la tabla periódica marcados con una X a continuación. No sólo garantiza parte del éxito en la asignatura, sino que es un entrenamiento estupendo para el cerebro, en un momento en el que ya ni siquiera memorizamos los números de teléfonos, por tenerlos en la agenda del móvil:
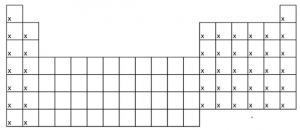
En la caracterización de la valencia tiene mucho que ver la cantidad de electrones que un elemento tiene en relación con el GAS NOBLE más cercano dentro de la tabla periódica. Es como si los gases nobles fueran los influencers de la química.
Todo esto tiene mucho que ver con los electrones que tiene el átomo, esto es, con la CONFIGURACIÓN ELECTRÓNICA DEL ÁTOMO de cada uno de los elementos:
Esa distribución de electrones, sigue el DIAGRAMA DE MOELLER:
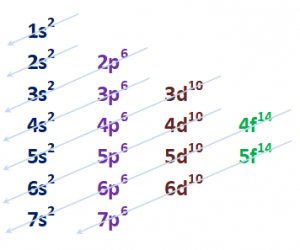
Que no deja de ser otro de los aspectos que se recoge en la TABLA PERIÓDICA:
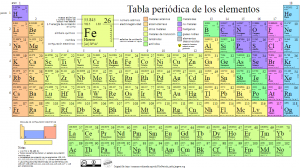
Así que intentemos descubrir las relaciones entre el DIAGRAMA DE MOELLER y la TABLA PERIÓDICA.
- Fijarse en 1s2, 2s2… (2 electrones)
- Fijarse en 2p6 … (6 electrones)
- En que los d tienen 10 electrones, los f 14 electrones
- Seguro que encuentras zonas de 2 en 2, de 6 en 6, de 10 en 10, de 14 en 14…
Debemos ser capaces de hacer las configuraciones electrónicas de los elementos, incluídos los iones (tener en cuenta que son los electrones lo que se gana o se pierde en un ión).
SEGUIR CON ENLACE QUÍMICO. RELACIONES INTERPERSONALES
PODRÍA SER DE INTERÉS IR A Ejercicios Resueltos de Estructura del Átomo para Física y Química de Secundaria
IR A CUADERNILLO DE FORMULACIÓN INORGÁNICA
PODRÍA INTERESAR LA VISITA AL SIGUIENTE ARTÍCULO DEL PROYECTO, DONDE SE DESARROLLAN LAS ASIGNATURAS DE FÍSICA Y QUÍMICA DE SECUNDARIA Y BACHILLERATO: